Aufgabe: man löst 0,3 L gasförmigen Chlorwasserstoff in Wasser; wieviel L einer Kalilauge (KOH) mit 0,1 mol/L benötigt man zur Neutralisation?
Wie man an die
Aufgabe herangeht
0. Konzentrieren, Sachen weglegen, die ablenken!
- Welche Formeln werden benötigt?
- Wie stelle ich die Gleichung auf?
- a) Wie berechne ich das Ergebnis?
b) Wie gebe ich das Ergebnis an?
zu 1.: Ich muss 3 Formeln auswendig können und wissen, wann/wofür ich sie brauche
Die Massenformel m = n × M; die Volumenformel Vgas = n × Vm und die Konzentrationsformel n = c × V
die Volumenformel gilt für Gase mit Vm = 22,4 L/mol, die Konzentrationsformel für gelöste Stoffe
da von gasf. HCl(g) und von Kalilauge, also einer wässrigen Lösung von Kaliumhydroxid die Rede ist, benötigt man
die Formel für das Gasvolumen und die Konzentrationsformel
zu 2.: Alle Berechnungen in der Stöchiometrie beruhen auf äquivalenten (dt.: gleichwertigen) Stoffmengen; Genaueres sagt
einem die Reaktionsgleichung: (hier)
1 HCl + 1 KOH ® KCl
+ H2O
Þ n(HCl) = n(KOH)
zu 3.: a) entweder Zahlen einsetzen und auf das richtige Ergebnis hoffen, oder besser Formeln verwenden und nach der
gesuchten Größe auflösen, dann erst die Zahlen einsetzen.
n(HCl) = V(HCl)/Vm(Gas)
n(KOH) = V(KOH) × c(KOH) Wieviel L Kalilauge Þ V(KOH) ist zu berechnen Gleichung umstellen
und wegen den äquivalenten Stoffmengen von Säure und Base gilt:
V(KOH) × c(KOH) = V(HCl)/Vm(Gas)
V(KOH) = V(HCl)/[Vm(Gas) × c(KOH)] / steht für den Bruchstrich oder für :
Zahlen am besten erst am Schluss einsetzen
V(KOH) = 0,3 L/[22,4 L/mol × 0,1 mol/L]
V(KOH) = 0,1339 L
b) Ergebnissatz schreiben: das gesuchte Volumen der 0,1 molaren Kalilauge beträgt 0,1339 Liter bzw. 133,9 mL
Was ist eine
Titration und wie führt man Titrationen rechnerisch durch
Der volle Name sagt bereits viel aus.
Titration: = Volumetrische Maßanalyse mit titrimetrischer Endpunkt-(=Äquivalenzpunkt)bestimmung
Volumina werden gemessen durch Zutropfen bis zur vollständigen Neutralisation
Versuchsaufbau, Aufgabenstellung: Bestimme die Konzentration der Analyse c(Anal.)
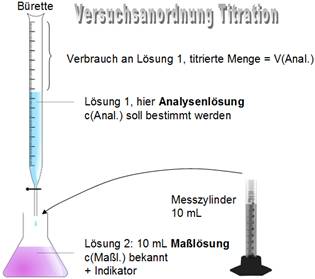
Versuchsdurchführung: Man lässt aus der Bürette solange die Lösung 1 zufließen bis der Indikator durch seinen
Farbumschlag den Endpunkt anzeigt, dann ist die Lösung neutral und enthält äquivalente Molmengen Säure und Base.
Auswertung, Rechung (Beispiel: HCl + NaOH ® H2O + NaCl)
Lösung 1 = Natronlauge = Analysenlösung: V1 = 25 mL; c1 = gesucht
Lösung 2 = Salzsäure = Maßlösung: V2 = 10 ml; c2 = 0,1 mol/L (auf dem Vorratsgefäß angegeben)
Am Äquivalenzpunkt gilt n1 = n2 Þ c1 × V1 = c2 × V2
Þ
c1 = ![]()
c1 = 0,1 mol/L × 10 mL : 25 mL
= 0,04 mol/L
Ergebnis: Die Natronlauge (Analyse) hat eine Konzentration von 0,04 mol/L
Ergänzung: Konduktometrische Titration
Bei dieser Variante wird der Endpunkt durch Leitfähigkeitsmessungen bestimmt, die Neutralisationsreaktion verändert die Leitfähigkeit so, dass diese immer geringer wird und am Äquivalenzpunkt minimal ist. Titriert man über den Endpunkt hinaus, steigt die Leitfähigkeit wieder
Zu Beginn (z.B) saure Lösung: Überschuss an H3O+
dann wird Lauge zugetropft: H3O+ + OH– ® H2O die zugegebenen OH– werden neutralisiert, H3O+ wird verbraucht
Am Äquivalenzpunkt: Leitfähigkeit sehr gering, nur noch
Autoprotolyse H2O ![]() H3O+ + OH– (minimale Mengen)
H3O+ + OH– (minimale Mengen)
Jenseits des Äquivalenzpunkts: die zugegebenen OH– werden nicht mehr neutralisiert, sondern erhöhen die Leitfähigkeit